Differenza chiave: la molitoria, nota anche come concentrazione molare, misura il numero di moli di una sostanza presente in ogni litro di soluzione. La molarità è indicata con un capitale M. Molality misura il numero di moli di una sostanza presente in ogni chilogrammo di solvente. La molalità è denotata con un minuscolo m.
Entrambi i concetti basano i loro calcoli su quante moli sono presenti nella soluzione corrente. Una soluzione può essere definita come una miscela omogenea, il che significa che due o più componenti sono stati mescolati al punto che non può essere distinto ad occhio nudo. Questi due concetti richiedono la comprensione delle talpe in quanto determina il numero di moli presenti nella soluzione. La teoria delle talpe fu scoperta dallo scienziato italiano Amedeo Avogardo.
Nel 1811, Avogardo propose che il volume di gas, ad una data temperatura e pressione, fosse proporzionale al numero di atomi o molecole indipendentemente dalla sua natura. Questo concetto è noto come costante di Avogardo. È definito come il numero di particelle costituenti (di solito atomi o molecole) in una mole di una determinata sostanza. In termini laici, una mole di una sostanza rappresenterebbe il numero di atomi e molecole presenti nell'elemento. Ad esempio: l'ossigeno ha un peso atomico di 16, questo rappresenterebbe la massa di mole di ossigeno. Quindi, una mole di ossigeno avrebbe una massa di 16 grammi. Secondo Avogardo, una mole di ossigeno avrebbe lo stesso numero di atomi di una mole di idrogeno. Tuttavia, possono differire in peso.
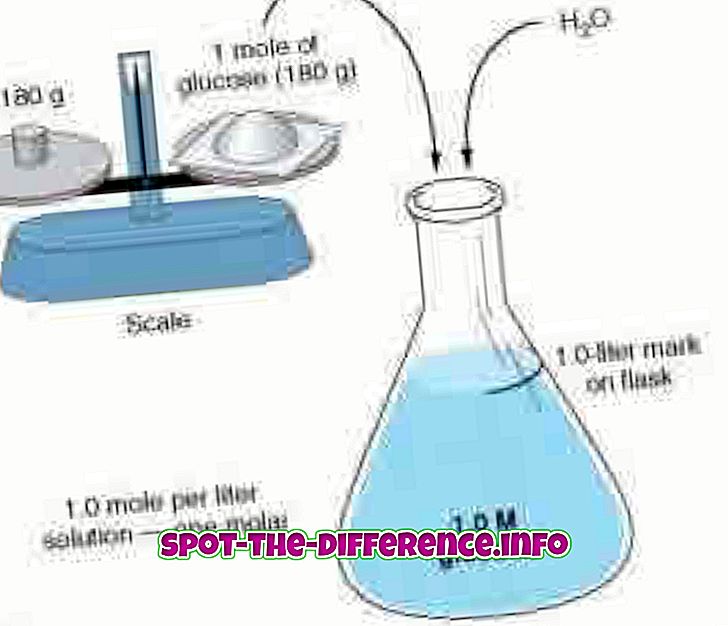
Molarità e molalità misurano la concentrazione utilizzando due diversi approcci. La molitoria, nota anche come concentrazione molare, misura il numero di moli di una sostanza presente in ogni litro di soluzione. La molarità è denotata con una M maiuscola. Quindi una soluzione con 1.0M affermerebbe che contiene 1 mole di soluto per litro di soluzione. Ad esempio: una soluzione di acqua e zucchero. Se la soluzione è misurata a 1, 0 M, la soluzione ha 1 mole di zucchero per litro di soluzione presente. La molitoria è anche nota come concentrazione della sostanza, concentrazione di quantità, concentrazione di sostanza o semplicemente concentrazione. La molarità può essere calcolata usando la formula: M = mol (n. Di moli) / L (volume di soluzione in litri).

La molalità misura il numero di moli di una sostanza presente in ogni chilogrammo di solvente. La molalità è denotata con un minuscolo m. Quindi una soluzione con 1.0m affermerebbe che contiene 1 mole di soluto per chilogrammo di solvente. Distinguiamo il soluto dal solvente. Il soluto è la sostanza che viene dissolta in un'altra sostanza. Un solvente è una sostanza che dissolve il soluto. Quindi, se l'acqua e lo zucchero sono mescolati insieme, lo zucchero sarebbe il soluto e l'acqua il solvente. L'acqua mista di zucchero sarebbe la soluzione. Ora, nella molalità, è della massima importanza che le talpe siano divise dalla massa del solvente e non dalla soluzione. La molalità può essere calcolata usando la formula: m = mol (numero di moli) / KG (massa di solvente in kg).
Perché la differenza? Bene, entrambi sono usati quando si tratta di temperatura. Se una soluzione sta per cambiare in temperatura, viene utilizzata la molalità. Ma per soluzioni che rimarranno a temperatura costante si usa la molarità. Questo perché quando la temperatura sale o scende, il volume della soluzione cambia e questo influenza direttamente la molarità. Quindi, la molalità viene utilizzata per calcolare la concentrazione.