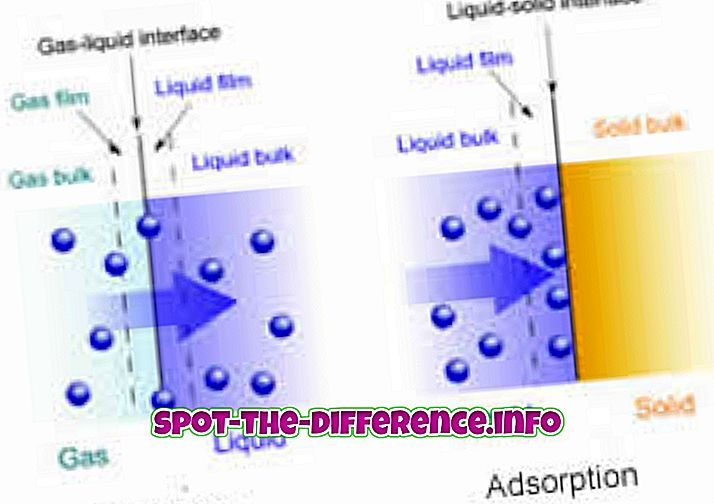
Differenza chiave: l' assorbimento è un fenomeno di massa in cui un assorbito penetra completamente nel corpo di un solido o di un liquido per formare un composto o una soluzione. D'altra parte, l'adsorbimento è un fenomeno superficiale in cui le molecole di un adsorbato si concen- trano solo sulla superficie di un adsorbente.
Reazione chimica - anidride carbonica assorbita da una soluzione di carbonio di potassio
Processo fisico - Aria assorbita in acqua mediante dissolvimento

Esistono due tipi di modalità di adsorbimento: chimico e fisico. Nell'assorbimento chimico, le molecole e la superficie sono legate dalle deboli forze di Vander Walls. D'altra parte, nell'adsorbimento chimico, si crea un legame chimico tra le molecole e la superficie.
Pertanto, la differenza principale tra adsorbimento e assorbimento è che l'assorbimento è un fenomeno di massa, il che significa che avviene in tutto il corpo del materiale, mentre l'adsorbimento rimane un fenomeno di superficie. L'adsorbimento è sempre esotermico, mentre l'assorbimento è endotermico. L'assorbimento comprende entrambi i processi di assorbimento e adsorbimento.
Confronto tra Adsorbimento e Assorbimento:
adsorbimento | Assorbimento | |
defintion | Accumulo di un gas o di un soluto liquido sulla superficie di un solido o di un liquido | Diffusione di una sostanza in un liquido o solido per formare una soluzione o composto |
Esempio | I gas inerti sono adsorbiti su carbone di legna. | Una spugna secca assorbe l'acqua |
Scambio di calore | Esotermico con eccezione di adsorbimento di H2 su vetro | Endotermico |
Raggiungere l'equilibrio | Comparativamente più veloce | Comparativamente lentamente |
Concentrazione | La concentrazione sulla superficie dell'adsorbente è diversa da quella della massa | La concentrazione rimane la stessa in tutto il materiale |
Tasso di accadimento | È rapido inizialmente ma in seguito il suo tasso inizia a diminuire | Si svolge a tasso uniforme |