Differenza chiave: in chimica, esotermica ed endotermica sono i due tipi principali di reazioni. Una reazione endotermica richiede calore (energia). D'altra parte, una reazione esotermica è quella che rilascia calore (energia). Quindi, entrambe le reazioni sono opposte l'una all'altra.
Ogni volta che le molecole interagiscono tra loro, avvengono varie reazioni. Queste reazioni sono classificate in molti gruppi in base alle loro caratteristiche o caratteristiche. Due di queste reazioni sono note come reazioni esotermiche ed endotermiche.

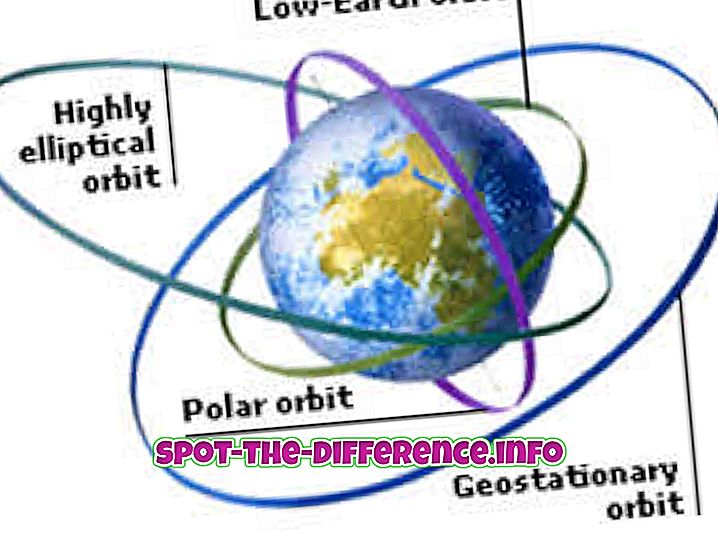
Uno degli esempi più comuni di queste reazioni è una reazione di fotosintesi in cui le piante assorbono energia dalla luce solare e quindi convertono l'anidride carbonica e l'acqua in ossigeno e zucchero. Il contenuto energetico dei reagenti in questo caso è inferiore ai prodotti.

Le due reazioni possono essere semplicemente comprese dalle equazioni. Supponiamo che dopo una reazione, una molecola generi la molecola B e C. L'energia di A rimane maggiore dell'energia totale di B e C. In questo caso, l'energia eccessiva verrà rilasciata nell'ambiente e la reazione sarà definita come una reazione esotermica.
A ---> B + C + energia
(reagenti) (prodotti)
Allo stesso modo, può essere rappresentata anche una reazione endotermica. Supponiamo che A abbia bisogno di prendere un po 'di energia dall'ambiente circostante per formare il prodotto D. Quando la molecola A prende energia dall'ambiente circostante, allora quel particolare ambiente diventa più freddo dopo la reazione. La fusione del ghiaccio è un esempio di reazione endotermica.
A + energia ---> D
(reagenti) (prodotto)
Confronto tra esotermico ed endotermico:
esotermico | Endotermico | |
Definizione | Una reazione esotermica è esattamente l'opposto di una reazione endotermica in quanto produce calore. | Una reazione endotermica è quel tipo di reazione che richiede o ha bisogno di energia. Questa energia viene fornita dall'ambiente circostante. |
Equazione simbolica | A -> B + C + energia | A + energia -> D |
Esempi |
|
|
Contenuto energetico | Il contenuto energetico dei prodotti è superiore a quello dei reagenti | Il contenuto energetico dei reagenti è inferiore ai prodotti |