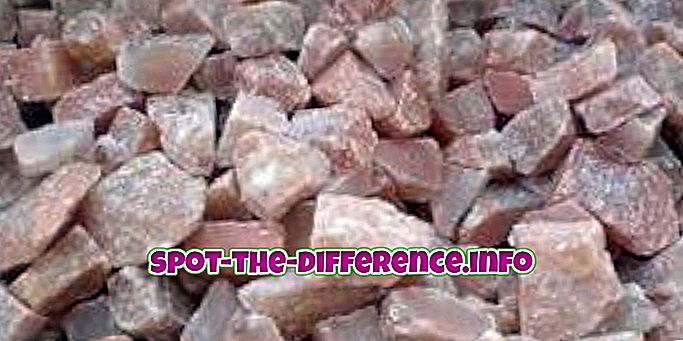
Differenza fondamentale: gli acidi e le basi sono due tipi di sostanze corrosive. Qualsiasi sostanza con un valore di pH compreso tra 0 e 7 è considerata acida, mentre un valore di pH compreso tra 7 e 14 è una base. Gli acidi sono composti ionici che si rompono in acqua per formare uno ione idrogeno (H +). I composti ionici sono composti con carica positiva o negativa. Le basi, d'altra parte sono composti ionici che si separano per formare uno ione idrossido di carica negativa (OH-) in acqua.

Tutti i composti chimici hanno un valore di pH. La scala del pH varia da 0 a 14. È la misura della concentrazione di ioni idrogeno in una soluzione. Qualsiasi sostanza al di sopra del pH neutro è considerata una base, mentre qualsiasi sostanza al di sotto del pH neutro è considerata un acido. Il pH neutro è il pH dell'acqua pura, cioè 7. Quindi, qualsiasi sostanza con un valore di pH compreso tra 0 e 7 è considerata acida, mentre un valore pH compreso tra 7 e 14 è una base.
Gli acidi sono composti ionici che si rompono in acqua per formare uno ione idrogeno (H +). I composti ionici sono composti con carica positiva o negativa. Le basi, d'altra parte sono composti ionici che si separano per formare uno ione idrossido di carica negativa (OH-) in acqua. La forza di un acido o base è determinata sulla base di quanti dei loro rispettivi ioni rilasciano; più ioni, più forti sono.
Inoltre, se si combinano acidi e basi con gli stessi punti di forza, tendono a produrre un sale e acqua. Ad esempio: HCl (acido) + NaOh (base) = NaCl (sale domestico) + H2O (acqua)
Caratteristiche degli acidi:
- gusto acido quando vengono mangiati
- può pungere la pelle quando vengono toccati
- può corrodere (o consumare) metalli e pelle
- può essere usato come reagente durante l'elettrolisi a causa della presenza di ioni mobili
- trasformare la carta blu tornasole rossa
- sono studiati in chimica e biologia
- diventa rosso o arancione sull'indicatore universale
Gli acidi possono essere classificati in:
- Acidi forti - i più comuni sono acido solforico, acido nitrico e acido cloridrico (H2SO4, HNO3 e HCl, rispettivamente).
- Alcuni acidi deboli concentrati, ad esempio acido formico e acido acetico
- Acidi forti di Lewis come cloruro di alluminio anidro e trifluoruro di boro
- Acidi di Lewis con reattività specifica, ad es. Soluzioni di cloruro di zinco
- Acidi estremamente forti (superacidi)

- Gusto amaro (contrario al gusto aspro degli acidi)
- Sensazione viscida o insaponata sulle dita
- Molte basi reagiscono con acidi e sali precipitati.
- Basi forti possono reagire violentemente con gli acidi. Una fuoriuscita acida può essere neutralizzata in modo sicuro utilizzando una base delicata.
- Le basi si trasformano in carta tornasole rossa blu
- Le basi sono sostanze che contengono ossidi o idrossidi metallici
- Basi solubili in acqua formano alcali (basi solubili)
Le basi possono essere classificate in:
- Caustiche o alcali, come idrossido di sodio (NaOH) e idrossido di potassio (KOH)
- I metalli alcalini sotto forma metallica (ad esempio sodio elementare) e gli idruri di metalli alcalini e alcalino-terrosi, come l'idruro di sodio, funzionano come basi forti e idratati per dare sostanze caustiche
- Basi estremamente forti (superbatteri) come alcossidi, ammidi metalliche (ad es. Ammide di sodio) e basi organometalliche come il butillitio
- Alcune basi deboli concentrate, come l'ammoniaca quando anidra o in una soluzione concentrata
Acido | Base | |
Definizione di Arrhenius | Un acido è un composto chimico che quando sciolto in acqua dà una soluzione con un'attività di ioni idrogeno maggiore rispetto all'acqua pura. | Una base è una sostanza acquosa che può accettare ioni di idrogeno. |
Bronstead Lowry Definition | Un acido è una sostanza che dona un protone. | Una base è qualsiasi sostanza che accetta un protone. |
valore del ph | Meno di 7.0 | Superiore a 7.0 |
Cartina tornasole | La cartina tornasole blu diventa rossa | la carta tornasole rossa diventa blu |
fenolftaleina | Rimane incolore | Rende la soluzione rosa |
Dissociazione (in acqua) | Acidi liberi di ioni idrogeno (H +) se miscelati con acqua. | Basa gli ioni idrossido (OH-) quando sono mescolati con acqua. |
Formula chimica | Un acido ha una formula chimica con H all'inizio di esso. Ad esempio, HCl (acido cloridrico). C'è un'eccezione alla sua regola, CH3COOH = Acetic Acid (aceto). | Una base ha una formula chimica con OH alla fine di esso. Ad esempio, NaOH (idrossido di sodio). |